
科学研究
1. 视路和脑干的神经胶质瘤
约有 15%~20%NF1 患者存在低分化胶质瘤,近 80% 出现在视觉通路,15% 出现在脑干,罕见于小脑、皮质和皮质下区域。视觉通路的胶质瘤(图 4A)常见于低于 7 岁的 NF1患儿。这些肿瘤以 WHO I 级胶质瘤(称为毛细胞星形细胞瘤)为主,病理上与非 NF1 患者的自发性胶质瘤难以鉴别。尽管许多视路胶质瘤无症状,但仍有半数可引起临床表现,最常见的为视力下降,一些患儿可出现性早熟。
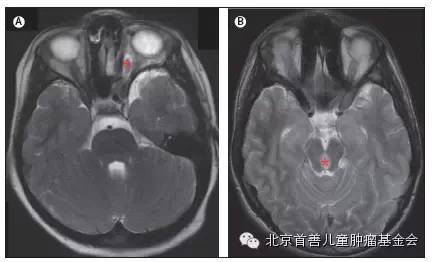
图 4. 低级别的胶质瘤。(A)MRI显示一名 4岁 NF1男性患儿的左侧视神经胶质瘤(星号)。(B)MRI显示一名 9岁 NF1男性患儿的脑干胶质瘤(星号)。
鉴于 NF1患儿视路胶质瘤发生的频率,所有 13岁以下的患儿都必须每年做眼动学检查;除非患儿不能完成眼科检查或无法做视敏度测量,否则不推荐做 MRI筛查。对于视胶质瘤的发现,目前推荐在第一年进行 4次眼科和 MRI检查,之后 2~3年逐渐延长检查的间隔时间,倘若标准视觉评估中视敏度两条线检查下降(如 Snellen图),则患儿需要转诊至儿科神经肿瘤专家进行治疗。
由于视路胶质瘤可引起永久的神经损伤,因此不适宜外科治疗。多数有症状的患者,一线治疗为卡铂联合长春新碱化疗,其它联合化疗方案也有应用,但尚无随机试验支持化疗方案中何种药物更佳。不推荐 NF1患者做颅脑放疗,因为该群体易于发生二次恶性肿瘤、血管异常和神经心理学障碍。
除视路之外,脑干是 NF1胶质瘤患者好发部位。与视路肿瘤相似,脑干胶质瘤(图 4B)常为毛细胞星形细胞瘤,但常出现在10 岁左右。患儿就诊时伴有颅内神经病变、嗜睡、步态不稳或头痛。卡铂或长春新碱化疗常用来治疗临床进展性肿瘤以及患儿其它低级别的胶质瘤。
2. 胶质母细胞瘤
根据一些病例报道和小型回顾性研究,NF1患者出现其它脑部肿瘤的风险至少增加了 5倍,包括 WHO IV级星形胶质细胞瘤(胶质母细胞瘤)。胶质母细胞瘤常见于年轻成人,预后极差。治疗与自发性胶质母细胞瘤相似,瘤体切除后辅助放疗和化疗(口服替莫唑胺)。
3. 恶性周围神经鞘膜瘤
恶性周围神经鞘膜瘤,也称为神经纤维肉瘤或神经源性肉瘤,是 Schwann细胞源性肉瘤的一种亚型。该肿瘤占全部软组织肉瘤的 3%~10%,在 NF1患者中占较大比率。恶性周围神经鞘膜瘤的一般人群和 NF1患者中的患病率分别为 0.001%和 0.1%,NF1患者发生该病的终生累积风险约为 8%~13%。
恶性周围神经鞘膜瘤可见于体内各处,已有丛状神经纤维瘤的部位,发生该病的风险增加了20倍;其它风险因素包括放射治疗史、整个 NF1基因胚系突变(微缺失)。
NF1患者若主诉有剧痛或疼痛难以控制、已有的丛状神经纤维瘤快速增大、肿瘤质地改变(由软变硬)或新的神经功能缺损,则应立即评估是否存在恶性周围神经鞘膜瘤。MRI有助于确定肿瘤的位置和大小,但无法鉴别肿瘤的良恶性。在过去十年中,新兴的¹⁸F-FDG-PET葡萄糖代谢检查,对发现恶性周围神经鞘膜瘤具有较高的敏感度和特异度。(图 5)。
穿刺活检可受样本偏倚的影响,令临床医师无法自信的确诊为恶性周围神经鞘膜瘤。此外,疑似恶变的患者应该接受转移癌的检查(如肺部、骨骼)。考虑到恶性周围神经鞘膜瘤具有进展性的特点,患者应接受包括神经病学家、放射学家、外科医师、肿瘤医师和肿瘤放疗专家在内的多学科治疗团队的评估和管理。

图 5. 1⁸F-FDG-PET 影像显示,一名 24岁 NF1女性患者(A)和一名 29岁 NF1男性患者(B)的恶性周围神经鞘膜瘤(星号)。
手术是恶性周围神经鞘膜瘤唯一的根治疗法,但手术切除后,患者的5 年总体生存率较差,该病是 NF1 患者主要的死因。研究提示,生存率已开始增加,尤其是女性患者;然而这种增加可能是由于对恶性周围神经鞘膜瘤认识和早期确诊的增多。
尽管放疗可延迟肿瘤复发,但并不能改变死亡的时间。辅助化疗仍有争议,一些病例中手术切除前行新辅助化疗,然而这类应用尚未广泛开展,目前针对恶性周围神经鞘膜瘤 NF1患者进行化疗的临床试验正在展开。对于与转移瘤的患者,蒽环霉素单药治疗是目前应用最多的姑息疗法。
非神经系统肿瘤
1. 胃肠道间质瘤
胃肠道间质瘤源自间充质细胞,可见于胃肠道任何部位。与普通人群相比(60 岁),NF1相关的胃肠道间质瘤患者较为年轻(平均年龄 50 岁),95% 的患者无症状。此外,有胃肠道间质瘤的 NF1 患者,与普通人群相比,出现多发性肿瘤的几率更高。
最常见的症状为腹痛、出血、肠穿孔和肠梗阻。胃肠道间质瘤可在影像学检查、手术切除其它肿瘤时偶然被发现,也可因出现临床症状而被确诊。
普通人群中,胃肠道间质瘤与 KIT 、 PDGFRA跨膜受体的表达增加有关,这些酪氨酸激酶受体的激活促进了细胞的增殖,是伊马替尼治疗的科学依据。相反,NF1 患者胃肠道间质瘤并不过表达 KI或 PDGFRA,限制了伊马替尼在此人群中的应用。目前,NF1相关胃肠道间质瘤的唯一治疗方案是手术。针对转移癌的其它酪氨酸受体抑制剂(如舒尼替尼)的临床试验正在开展中。
2. 乳腺癌
NF1患者乳腺癌的发生风险增加了 5倍,主要累及年逾 50岁的女性。此外,有乳腺癌的NF1女性患者,死亡率高于普通人群的乳腺癌女性患者。
尽管发表的研究纳入了少量的患者,但 NF1患者乳腺癌的相对风险与有乳腺癌家族史的人群相似。30~49岁的NF1女性患者,应尽早行钼靶 X线或MRI 检查;然而在推荐此类人群的乳腺癌筛查之前,需要进行大型前瞻性研究。目前,NF1相关的乳腺癌治疗与普通人群的乳腺癌治疗相同。
3. 白血病和淋巴瘤
NF1患儿发生髓性白血病的风险与普通儿童相比,增加了至少7 倍;慢性粒单核细胞白血病、幼年型粒 - 单核细胞白血病、急性淋巴细胞白血病和非霍奇金氏淋巴瘤的患病率亦有增加。然而,这些肿瘤在 NF1 患者中较为罕见。
此外,尚无证据支持NF1 相关白血病和普通人群白血病预后之间存在差异。NF1 相关白血病的治疗与普通人群白血病相同。
4. 嗜铬细胞瘤
嗜铬细胞瘤,是肾上腺髓质或交感神经系统其它部位的肿瘤,可分泌儿茶酚胺,在 NF1患者中发生率增加,约为 0.1%~5.7%,普通人群发生率为 0.002%~0.008%。NF1相关患者的起病的年龄(常为 40 ~50岁)与自发性患者相似。疑似嗜铬细胞瘤的 NF1患者,常出现无法解释的高血压、头痛、面部潮红、出汗或心悸。
诊断需要联合影像学检查(胸腹部CT/MRI,若 CT 阴性则间碘苄胍扫描、生长抑素显像)以及生化评估(如尿中儿茶酚胺水平)。如病灶可切除,则手术可治愈;对于无法切除或转移癌的患者,则可化疗或采用131碘- 间碘苄胍放射药物治疗。
5. 十二指肠类癌
十二指肠类癌是源自胃肠道内分泌细胞的神经内分泌肿瘤,据报道 NF1患者发生率为 1%,最常见的部位为十二指肠壶腹部,因此患者常有黄疸和非特异性腹痛。此病常见于年轻的NF1 患者。
十二指肠类癌的诊断需要临床联合影像学检查(如胸腹部和骨盆 CT、生长抑素成像、内镜超声或内窥镜)以及尿、血浆 5-羟色胺和嗜铬粒蛋白 A水平。
如有可能,应行手术切除;不能切除以及转移癌的患者一般予以生长抑素类似物治疗或化疗。
6. 横纹肌肉瘤
横纹肌肉瘤是非神经源性肉瘤,由来源于神经嵴的蓝染小圆形细胞组成,NF1患儿此病的发生风险增加了 20倍。横纹肌肉瘤多表现为可触性团块,治疗为手术切除,辅助化疗和放疗对部分患者有效。



